 |
| Ayo Belajar Apa Itu Koloid |
Pengantar
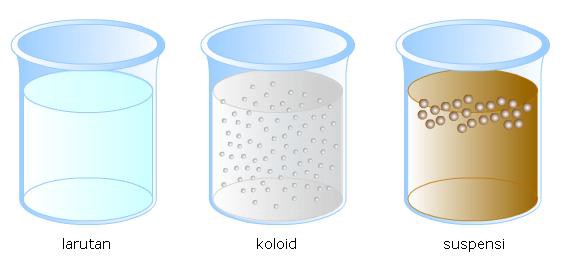
Sistem koloid adalah suatu bentuk campuran yang keadaannya terletak antara larutan dan suspensi (campuran kasar). Sistem koloid ini mempunyai sifat-sifat khas yang berbeda dari sifat larutan atau suspensi. Keadaan koloid bukan ciri dari zat tertentu karena semua zat, baik padat, cair, maupun gas, dapat dibuat dalam keadaan koloid. Sistem koloid sangat berkaitan erat dengan hidup dan kehidupan kita sehari-hari. Cairan tubuh, seperti darah adalah sistem koloid, bahan makanan seperti susu, keju, nasi, dan roti adalah sistem koloid. Cat, berbagai jenis obat, bahan kosmetik, tanah pertanian juga merupakan sistem koloid. Karena sistem koloid sangat berpengaruh bagi kehidupan sehari-hari, kita harus mempelajarinya lebih mendalam agar kita dapat menggunakannya dengan benar dan dapat bermanfaat untuk diri kita.
Sistem koloid adalah suatu bentuk campuran yang keadaannya terletak antara larutan dan suspensi (campuran kasar). Sistem koloid ini mempunyai sifat-sifat khas yang berbeda dari sifat larutan atau suspensi. Keadaan koloid bukan ciri dari zat tertentu karena semua zat, baik padat, cair, maupun gas, dapat dibuat dalam keadaan koloid. Sistem koloid sangat berkaitan erat dengan hidup dan kehidupan kita sehari-hari. Cairan tubuh, seperti darah adalah sistem koloid, bahan makanan seperti susu, keju, nasi, dan roti adalah sistem koloid. Cat, berbagai jenis obat, bahan kosmetik, tanah pertanian juga merupakan sistem koloid. Karena sistem koloid sangat berpengaruh bagi kehidupan sehari-hari, kita harus mempelajarinya lebih mendalam agar kita dapat menggunakannya dengan benar dan dapat bermanfaat untuk diri kita.
Cara Pembuatan Koloid
1. Kondensasi yaitu pembuatan koloid dengan mengubah partikel-partikel larutan
yang terdiri dari molekul-molekul atau ion menjadi partikel koloid.
Cara kondensasi merupakan cara kimia, misalnya :
a. Reaksi redoks : 2H2S(g) + SO2(aq) → 2H2O(l) + 3S(koloid)
b. Reaksi Hidrolisis : FeCl3(aq) + 3H2O(l)--> → Fe(OH)3(koloid) +3HCl(aq)
c. Reaksi dekomposisi rangkap : AgNO3(aq) + NaCl(aq) → AgCl(koloid) + NaNO3(aq)
d. Reaksi pergantian pelarut : S + alkohol + air → S(koloid)
2. Cara Dispersi yaitu pembuatan koloid dari suspensi kasar. Cara dispersi dibedakan menjadi 4, yaitu :
a. Cara Mekanik
Pembuatan koloid dengan cara penggerusan/penggilingan untuk zat padat, cara
pengadukan/pengocokan untuk zat cair, kemudian didispersikan ke dalam medium (pendispersi).
Contoh : belerang halus + air → sol belerang
b. Cara Peptisasi
Pembuatan koloid dengan cara memecah molekul besar menjadi molekul yang lebih kecil
dengan menghilangkan ion elektrolit penyebab gumpalan.
c. Cara Busur Bredig (Elektrodispersi)
Pembuatan koloid dengan menggunakan loncatan bunga api listrik. Cara ini biasanya untuk membuat sol logam.
d. Cara Homogenisasi
Pembuatan koloid dengan cara membuat suatu zat menjadi homogen dan berukuran koloid. Cara ini digunakan pada pembuatan susu.
Klasifikasi Campuran
Cara kondensasi merupakan cara kimia, misalnya :
a. Reaksi redoks : 2H2S(g) + SO2(aq) → 2H2O(l) + 3S(koloid)
b. Reaksi Hidrolisis : FeCl3(aq) + 3H2O(l)--> → Fe(OH)3(koloid) +3HCl(aq)
c. Reaksi dekomposisi rangkap : AgNO3(aq) + NaCl(aq) → AgCl(koloid) + NaNO3(aq)
d. Reaksi pergantian pelarut : S + alkohol + air → S(koloid)
2. Cara Dispersi yaitu pembuatan koloid dari suspensi kasar. Cara dispersi dibedakan menjadi 4, yaitu :
a. Cara Mekanik
Pembuatan koloid dengan cara penggerusan/penggilingan untuk zat padat, cara
pengadukan/pengocokan untuk zat cair, kemudian didispersikan ke dalam medium (pendispersi).
Contoh : belerang halus + air → sol belerang
b. Cara Peptisasi
Pembuatan koloid dengan cara memecah molekul besar menjadi molekul yang lebih kecil
dengan menghilangkan ion elektrolit penyebab gumpalan.
c. Cara Busur Bredig (Elektrodispersi)
Pembuatan koloid dengan menggunakan loncatan bunga api listrik. Cara ini biasanya untuk membuat sol logam.
d. Cara Homogenisasi
Pembuatan koloid dengan cara membuat suatu zat menjadi homogen dan berukuran koloid. Cara ini digunakan pada pembuatan susu.
Klasifikasi Campuran
|
Larutan
|
Koloid
|
Suspensi Kasar
|
|
- Homogen, tdk dapat dibedakan dengan mikroskop ultra
- Jernih
- satu fase
- Tidak dapat disaring
- Tidak memisah (stabil)
- Diameter partikel
<>-7 cm
|
- Tampak homogen, dgn mikroskop ultra tampak heterogen
- Tidak jernih
- Dua fase
- Dapat disaring kertas saring ultra
- Umumnya stabil
- Diameter partikel 10-7 -10-5 cm.
|
- Heterogen
- Tidak jernih
- Dua fase
- Dapat disaring kertas saring ultra
- Tidak stabil
- Diameter partikel
> 10-5cm
|
Sistem Koloid
Sistem koloid dibagi menjadi dua bagian yaitu fase terdispersi (zat terlarut) dan medium
pendispersi (pelarut). Keduanya terdiri dari tiga fase/wujud yaitu padat, cair dan gas yang bersatu. Namun antara fase gas dengan gas tidak membentuk Sistem koloid karena bercampur homogen, melainkan larutan
|
No
|
Fase Terdispersi
|
Medium Pendispersi
|
Nama Koloid
|
Contoh
|
|
1.
|
Padat
|
Padat
|
Sol Padat
|
Perunggu, baja
|
|
2.
|
Padat
|
Cair
|
Sol
|
Cat, tinta, lotion
|
|
3.
|
Padat
|
Gas
|
Aerosol padat
|
Asap, debu diudara
|
|
4.
|
Cair
|
Padat
|
Emulsi Padat
|
Keju, mentega, jeli
|
|
5.
|
Cair
|
Cair
|
Emulsi cair
|
Susu, santan
|
|
6.
|
Cair
|
Gas
|
Aerosol cair
|
Kabut, awan
|
|
7.
|
Gas
|
Padat
|
Busa
|
Batu apung, busa jok
|
|
8.
|
Gas
|
Cair
|
Busa/buih
|
Buih sabun/sampo
|
Sifat-Sifat Koloid
1. Efek
Tyndall
Efek tyndall ini ditemukan oleh John Tyndall (1820-1893), seorang ahli fisika
Inggris. Oleh karena itu sifat itu disebut efek tyndall. Efek tyndall adalah
efek yang terjadi jika suatu larutan terkena sinar. Pada saat larutan sejati
disinari dengan cahaya, maka larutan tersebut tidak akan menghamburkan cahaya,
sedangkan pada sistem koloid, cahaya akan dihamburkan. hal itu terjadi karena partikel-partikel
koloid mempunyai partikel-partikel yang relatif besar untuk dapat menghamburkan
sinar tersebut. Sebaliknya, pada larutan sejati, partikel-partikelnya relatif
kecil sehingga hamburan yang terjadi hanya sedikit dan sangat sulit diamati.
2. Gerak Brown
Gerak Brown adalah gerak acak, gerak tidak beraturan dari partikel koloid.
Jika kita amati sistem koloid dibawah mikroskop ultra, maka kita akan melihat bahwa partikel-partikel tersebut akan bergerak membentuk zigzag. Pergerakan zigzag ini dinamakan gerak Brown Partikel – partikel suatu zat senantiasa bergerak. Gerakan tersebut bersifat acak seperti pada zat cair dan gas. System koloid dengan medium pendipersi zat cair atau gas, partikel-partikel menghasilkan tumbukan. Tumbukan tersebut berlangsung dari segala arah. Partikel koloid cukup kecil, tumbukan cenderung tidak seimbang. Dan menyebabkan perubahan arah partikel sehingga terjadi gerak zigzag atau gerak brown. Semakin kecil ukuran partikel koloid, semakin cepat gerak brown. Semakin besar ukuran partikel, semakin lambat gerak brown.
Gerak Brown dipengerahui oleh suhu. Semakin tinggi suhu system, koloid, semakin besar energi kinektik yang dimiliki partikel medium. Akibatnya, gerak Brown dari partikel fase terdispersinya semakin cepat. Semakin rendah suhu system koloid, maka gerak Brown semakin lambat.
 |
| Elektroforesis |
3. Elektroforesis
Oleh karena partikel sol bermuatan listrik, maka partikel ini akan bergerak dalam medan listrik. Pergerakan ini disebut elektroforesis. Untuk lebih jelas, mari kita lihat tabung berikut di samping. Pada gambar, terlihat bahwa partikel-partikel koloid bermuatan positif tersebut bergerak menuju elektrode dengan muatan berlawanan, yaitu elektroda negatif. Jika sistem koloid bermuatan negative, maka partikel itu akan menuju ke elektroda positif.
Manfaat elektroforesis adalah :
a. Menerima muatan yang dimiliki suatu partikel.
b. Memproduksi barang industri yang terbuat dari karet, misalnya sarung tangan.
c. Mengurang zat pencemar udara yang dihasilkan dunia industri dengan metode Cottrell.
a. Menerima muatan yang dimiliki suatu partikel.
b. Memproduksi barang industri yang terbuat dari karet, misalnya sarung tangan.
c. Mengurang zat pencemar udara yang dihasilkan dunia industri dengan metode Cottrell.
 |
| Koagulasi |
4. Koagulasi
Jika partikel-partikel koloid tersebut bersifat netral, maka akan terjadi penggumpalan dan pengendapan karena pengaruh gravitasi. Proses penggumpalan dan pengendapan ini disebut koagulasi. Koagulasi yaitu peristiwa pengendapan partikel-partikel koloid sehingga fase terdispersinya terpisah dari medium pendispersinya. Koagulasi disebabkan karena hilangnya kestabilan untuk mempertahanKan partikel agar tetap tersebar di medium pendispersi. Koagulasi dapat dilakukan dengan penambahan zat elektrolit dan cara mekanik ( pemanasan, pendinginan, pengadukan ).
Kegunaan koagulasi adalah :
a. Penjernihan air dengan penambahan tawas (K2SO4.Al(SO4)3).
b. Proses pendinginan santan.
c. Pengolahan karet dari lateks.
d. Pembentukan delta di daerah muara sungai.
e. Telur rebus dan pembuatan agar-agar.
5. Adsorpsi
a. Penjernihan air dengan penambahan tawas (K2SO4.Al(SO4)3).
b. Proses pendinginan santan.
c. Pengolahan karet dari lateks.
d. Pembentukan delta di daerah muara sungai.
e. Telur rebus dan pembuatan agar-agar.
5. Adsorpsi
Partikel sol padat ditempatkan dalam zat cair atau gas, maka partikel zat cair atau gas akan terakumulasi. Fenomena disebut adsorpsi. Jadi sdsorpsi terkait dengan penyerapan partikel pada permukaan zat. Partikel koloid sol memiliki kemampuan untuk mengadsorpsi partikel pendispersi pada permukaanya. Daya adsorpsi partikel koloid tergolong besar Karenna partikelnya memberikan sesuatu permukaan yang luas. Sifat ini telah digunakan dalam berbagai proses seperti penjernihan air.
Manfaat adsorpsi adalah :
1. Penggunaan norit untuk penyembuhan sakit perut.
2. Proses pemutihan gula pasir pada industri gula dengan tanah diatomi dan arang tulang.
3.Pewarnaan serat sutra, wool atau kapas dalam larutan Al2(SO4)3 pada industri tekstil.
4. Proses penjernihan air keruh dengan tawas.
5. Pembersihan kotoran dengan sabun.
6. Adsorpsi koloid humus oleh koloid tanah liat.
Koloid Liofil dan Liofob
1. Penggunaan norit untuk penyembuhan sakit perut.
2. Proses pemutihan gula pasir pada industri gula dengan tanah diatomi dan arang tulang.
3.Pewarnaan serat sutra, wool atau kapas dalam larutan Al2(SO4)3 pada industri tekstil.
4. Proses penjernihan air keruh dengan tawas.
5. Pembersihan kotoran dengan sabun.
6. Adsorpsi koloid humus oleh koloid tanah liat.
Koloid Liofil dan Liofob
|
No
|
Koloid Liofil
|
Koloid Liofob
|
|
1.
|
Stabil
|
Kurang stabil
|
|
2.
|
Kekentalan
tinggi
|
Kekentalan rendah
|
|
3.
|
Dapat
dibuat gel
|
Tidak semua dapat dibuat gel
|
|
4.
|
Sukar
diendapkan
|
Mudah diendapkan
|
|
5.
|
Mengadsorpsi
molekul
|
Mengabsorpsi ion
|
|
6.
|
Kurang
menunjukkan efek Tyndall
|
Efek Tyndall sangat jelas
|
|
7.
|
Dibuat
dengan cara dispersi
|
Dibuat secara kondensasi
|
|
8.
|
Gerak
Brown kurang jelas
|
Gerak Brown sangat jelas
|
|
9.
|
Terdiri
dari zat organik
|
Terdiri dari zat organik
|
|
10.
|
Reversibel
|
Tidak reversibel
|
Penjernihan Air
Air keran (PDAM) yang ada saat ini mengandung partikel-partikel koloid tanah liat,lumpur, dan berbagai partikel lainnya yang bermuatan negatif. Oleh karena itu, untuk menjadikannya layak untuk diminum, harus dilakukan beberapa langkah agar partikel koloid tersebut dapat dipisahkan. Hal itu dilakukan dengan cara menambahkan tawas (Al2SO4)3.Ion Al3+ yang terdapat pada tawas tersebut akan terhidroslisis membentuk partikel koloid Al(OH)3 yang bermuatan positif melalui reaksi:
Al3+ + 3H2O → Al(OH)3 + 3H+
Setelah itu, Al(OH)3 menghilangkan muatan-muatan negatif dari partikel koloid tanah liat/lumpur dan terjadi koagulasi pada lumpur. Lumpur tersebut kemudian mengendap bersama tawas yang juga mengendap karena pengaruh gravitasi.











Comments
Post a Comment