Belajar Kimia-Ikatan adalah sesuatu yang menghubungkan sesuatu hal dengan hal yang lain. Dalam kehidupan sehari-hari selalu ada ikatan antara sesama manusia. Misalnya ikatan antara kakak dan adik dalam keluarga, guru dan murid, bapak dan anak . Dalam ikatan kimia ada ikatan yang menghubungkan unsur-unsur untuk membentuk suatu senyawa. Ikatan ini terbentuk agar unsur-unsur mengalami kestabilan.
Jenis-Jenis Ikatan :
Ikatan Ion
Ikatan Kovalen
Ikatan Kovalen Koordinasi
Ikatan Logam
Jenis-Jenis Ikatan :
Ikatan Ion
Ikatan Kovalen
Ikatan Kovalen Koordinasi
Ikatan Logam
Kestabilan Atom
Tujuan pembentukan ikatan kimia adalah agar terjadi pencapaian kestabilan suatu unsur.
Elektron yang berperan pada pembentukan ikatan kimia adalah elektron valensi dari suatu atom/unsur yang terlibat.
Tujuan pembentukan ikatan kimia adalah agar terjadi pencapaian kestabilan suatu unsur.
Elektron yang berperan pada pembentukan ikatan kimia adalah elektron valensi dari suatu atom/unsur yang terlibat.
Teori Oktet dan Duplet
W Kossel dan G.N Lewis berpendapat atom disebut stabil jika mempunyai konfigurasi elektron mirip gas mulia yaitu pada kulit terakhir mempunyai 8 elektron (oktet) atau 2 elektron (duplet jika jumlah kulit hanya 1) Salah 1 petunjuk dalam pembentukan ikatan kimia adalah adanya 1 golongan unsur yang stabil yaitu golongan VIIIA atau golongan 18 (gas mulia). Maka dari itu, dalam pembentukan ikatan kimia; atom-atom akan membentuk konfigurasi elektron seperti pada unsur gas mulia.
W Kossel dan G.N Lewis berpendapat atom disebut stabil jika mempunyai konfigurasi elektron mirip gas mulia yaitu pada kulit terakhir mempunyai 8 elektron (oktet) atau 2 elektron (duplet jika jumlah kulit hanya 1) Salah 1 petunjuk dalam pembentukan ikatan kimia adalah adanya 1 golongan unsur yang stabil yaitu golongan VIIIA atau golongan 18 (gas mulia). Maka dari itu, dalam pembentukan ikatan kimia; atom-atom akan membentuk konfigurasi elektron seperti pada unsur gas mulia.
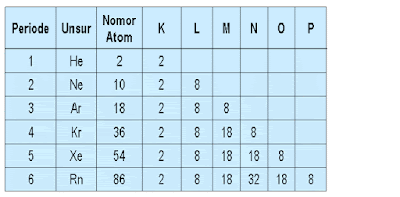
Unsur gas mulia mempunyai elektron valensi sebanyak 8 (oktet) atau 2 (duplet, yaitu atom Helium).
Kecenderungan unsur-unsur untuk menjadikan konfigurasi elektronnya sama seperti gas mulia terdekat dikenal dengan istilah Aturan Oktet
Ikatan yang terjadi antar atom atau antar molekul dengan cara sebagai berikut :
a) atom yang 1 melepaskan elektron, sedangkan atom yang lain menerima elektron
(serah terima elektron)
1. Melepaskan elektron
contoh: 11Na : 2.8.1 (tdk stabil) → 11Na+ : 2.8 (stabil) + e
12 Mg : 2.8.2 (tdk stabil) → 12Mg+2 : 2.8 (stabil) + 2e
Berlaku untuk atom yang mempunyai elektron valensi 2 atau 1
2. Menangkap elektron
contoh: 9F : 2.7 (tidak stabil) + e → 9F- : 2.8 (stabil)
8O : 2.6 (tidak stabil) + 2e → 8O-2 :2.8 (stabil)
Berlaku untuk atom yang mempunyai elektron valensi 6 atau 7
b) Penggunaan bersama pasangan elektron yang berasal dari masing-masing atom yang berikatan. Terjadi pada atom-atom yang mempunyai energi ionisasi yang tinggi sehingga sukar melepaskan elektron dan yang mempunyai afinitas elektron rendah sehingga sukar mengikat elektron.
cont : HF
1H :1 (belum stabil) stabil setelah disumbang 1elektron dari Cl
17Cl : 2.8.7 (belum stabil)stabil setelah disumbang 1 elektron dari H
Melukis Struktur Lewis
Titik-titik mewakili elektron valens ini diisi satu persatu dahulu; biasanya dalam urutan:
dari kanan ke kiri kemudian ke atas dan bawah, sehinggalah kesemua empat sukuan tersebut berisi dengan satu elektron. Elektron ke-5 seterusnya akan diisikan secara berpasangan.
Titik-titik mewakili elektron valens ini diisi satu persatu dahulu; biasanya dalam urutan:
dari kanan ke kiri kemudian ke atas dan bawah, sehinggalah kesemua empat sukuan tersebut berisi dengan satu elektron. Elektron ke-5 seterusnya akan diisikan secara berpasangan.