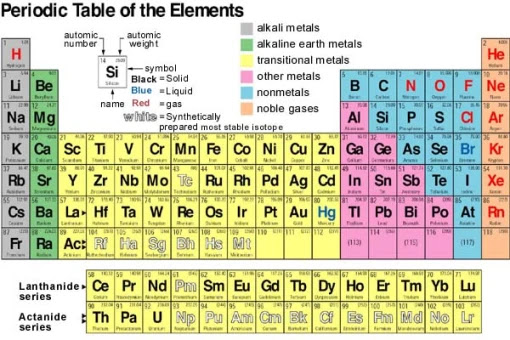
Belajar Kimia- Sifat Keperiodikan unsur dalam sistem periodik dapat dijelaskan sebagai berikut:
- Unsur yang terdapat dalam golongan yang sama memiliki kemiripan konfigurasi elektron, maka unsur yang segolongan mempunyai sifat yan mirip.
- Unsur yang terdapat dalam satu periode dari kiri ke kanan , konfigurasinya berubah secara teratur, sehingga dalam satu periode dari kiri ke kanan mempunyai sifat yang berubah secara teratur.
Sfat Keperiodikan unsur dalam sistem periodik meliputi:
a. Jari-jari atom
- JAri-jari atom adalah jarak inti atom dengan elektron pada kulit terluar.
- Dalam satu periode, dari kiri ke kanan jari-jari makin kecil. Hal ini disebabkan karena dalam satu periode, julmlah kulit sama tetapi muatan inti bertambah banyak sehingga daya tarik inti dengan elektron semakin kuat.
- Dalam satu golongan, dari atas kebawah, jari-jari makin besar kerena jumlah kulit semakin banyak
b. Energi
Ionisasi
- Energi ionisasi adalah besarnya energi yang diperlukan untuk melepaskan satu elektronya yang terikat paling lemah oleh suatu atom atau ion dalam keadaan gas.
- Dalam satu periode, dari kiri ke kanan energi ionisasi makin besar. Hal ini disebabkan gaya tarik inti semakin besar energi yang diperlukan untuk melepaskan elektron yang terikat paling lemah.
- Dalam satu golongan, dari atas kebawah energi ionisasi semakin kecil. Karena gaya tarik inti terhadap elektron pada kulit terluar makin lemah, maka energi yang diperlukan untuk melepaskan elektron semakin sedikit.
c. Afinitas
elektron
- Afinitas elektron adalah besarnya energi yang dihasilkan atau dilepaskan apabila atom unsur dalam fase gas menarik elektron.
- Dalam satu periode, dari kiri ke kanan afinitas elektron makin besar. hal ini disebabkan gaya tarik inti besar sehingga atom makin mudah menagkap elektron yang menyebabkan makin banyak energi yang dilepaskan.
- Dalam satu golongan, dari atas ke bawah afinitas elektron makin kecil. Karena gaya tarik inti makin lemah maka atom makin sulit menangkap elektron yang mengakibatkan makin sedikit energi yang dibebaskan.
d.
Keelektronegatifan
- Keelektronegatifan adalah kecenderungan atom dalam menarik pasangan elektron yang digunakan bersama dalam membentuk ikatan
- Semakin besar harga keelektronegatifan suaty atom, semakin mudah bagi atom tersebut untuk menarik pasangan elektron ikatan atau gaya tarik elektron dari atom tersebut semakin kuat.
- Pola kecenderngannya sama dengan afinitas elektron, dan mempunyai makna yang berlawanan dengan energi ionisasi.
e.
Sifat Logam dan Nonlogam
Dalam sistem periodik unsur logam
terletak di sebelah kiri dan unsur nonlogam terletak di sebelah kanan. Dalam
suatu perioda dari kiri ke kanan, sifat kelogaman berkurang sedangkan dalan dari satu
golongan dari atas kebawah sfat kelogaman semakin besar
f. Titik leleh dan titik didih
Titik leleh dan titk didih termasuk sifat fisis. Unsur logam dalam suatu golongan dari atas ke bawa, titik leleh dan titik didihnya cenderung makin rendah, sedangkan unsur non golongan cenderung makin tinggi. dalam suatu periode dari kiri kekanan , titik lelehnya naik sampai maksimum golongan IVA kemudian turun secara teratur, sedangkan titik didih naik sampai maksimum golongan IIIA, kemudian turun secara teratur.